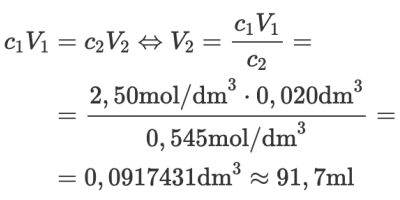Tid: 90 minuter
Tillåtna hjälpmedel: Miniräknare, medföljande periodiskt system.
Hoppa direkt till …
Del I. Frågor som bara kräver ett kort svar (ett ord eller 1–2 meningar)
Längre svar ger risk för avdrag.
- Vanillin är ett ämne som ger vanilj dess karakteristiska doft. Summaformeln för vanillin är C8H8O3. Beräkna molekylmassan för vanillin. (1p)
- Hur stor substansmängd är det i 3,25 g vanadium(III)bromid, VBr3? (1p)
- När propan (C3H8) förbränns i luft bildas koldioxid och vatten. Skriv en balanserad reaktionsformel för reaktionen. (1p)
- Kvävedioxid (NO2) kan reagera med vatten (H2O). Då bildas ammoniak (NH3) och syrgas (O2) enligt nedanstående reaktionsformel:
4NO2 + 6H2O → 4NH3 + 7O2
Hur stor substansmängd syrgas bildas om 9,78 mol kvävedioxid får reagera? (1p)
Del II. Ringa in de rätta svaren
Tips 1: Läs igenom alla svarsalternativen innan du bestämmer dig för vilket alternativ som är korrekt.
Tips 2: Om det är någon eller några frågor som du inte kan lösa direkt eller nästan direkt, så hoppa över dem så länge. Återkom till de frågorna senare, så vet du hur mycket tid du kan disponera på dem.
- Bensin består av en blandning på olika kolväten med 5–10 kolatomer. Vilket av följande ämnen förväntas lösa sig bäst i bensin? Ringa in ett alternativ (1p).
- Koncentrerad saltsyra (HCl).
- Strösocker (C12H22O11).
- Vanligt koksalt (NaCl).
- Matolja (fettmolekyler).
- Kvarts (SiO2) har en extremt hög smältpunkt (cirka 1700 °C). Till skillnad från koldioxid (CO2) bildar kiseldioxid ett tredimensionellt nätverk av kisel- och syreatomer. Kisel har en elektronegativitet på 1,8 och syre 3,4. Vilken typ av bindningar måste brytas för att kvarts ska smälta? Ringa in ett alternativ (1p).
- van der Waals-bindningar
- Kovalenta bindningar
- Metallbindningar
- Dipol–dipol-bindningar
- Betrakta följande fyra ämnen: metan (CH4), ammoniak (NH3), vätesulfid (H2S) och vätefluorid (HF). Mellan vilka av dessa ämnens molekyler är vätebindningar den dominerande intermolekylära bindningen i vätskefas? Ringa in ett alternativ (1p).
- Endast mellan HF-molekyler.
- Mellan alla fyra eftersom alla innehåller väteatomer.
- Mellan NH3-, H2S- och HF-molekyler.
- Mellan NH3-molekyler och mellan HF-molekyler.
- För de flesta salter, som kaliumnitrat (KNO3), ökar lösligheten markant när temperaturen stiger. Vad är den främsta kemiska orsaken till detta i relation till bindningar? Ringa in ett alternativ (1p).
- Uppvärmningen gör att de kovalenta bindningarna i saltet blir mer polära, vilket stärker attraktionskraften till vattnets dipoler.
- Värmen gör att vattenmolekylerna krymper, vilket gör att fler joner får plats mellan dem i de tomma hålrummen i vätskan.
- Vattenmolekylerna börjar rotera så snabbt att de skapar ett magnetfält som drar ut jonerna ur den fasta fasen mer effektivt.
- Vid högre temperatur ökar jonernas rörelseenergi, vilket gör att jonbindningarna i saltet lättare bryts.
- Vilken typ av intermolekylär bindning är den starkaste som verkar mellan två HCl-molekyler i flytande eller fast form? Ringa in ett alternativ (1p).
- van der Waals-bindning
- Jonbindning
- Metallbindning
- Dipol–dipol-bindning
- Geckoödlor (se bilden nedan till vänster) har en makalös förmåga att klättra på släta väggar, och kan till och med klättra på lodrätt glas. Detta beror inte på sugkoppar eller något klibbigt ämne, utan på att deras fotsulor (se bilden nedan till höger) är beklädda med miljontals små hår, som binder till glasväggens yta.
 Geckoödla.
Geckoödla.Geckoödlans fotsula.
Vilken typ av bindning är huvudsakligen ansvarig för denna fästförmåga? Ringa in ett alternativ. (1p)- Starka jonbindningar mellan positiva och negativa laddningar.
- Summan av ett enormt antal svaga van der Waals-bindningar.
- Vätebindningar mellan vattenmolekyler på ödlans fot och på glasytan.
- Kovalenta bindningar som bildas mellan ödlans fot och glasytan.
- Koldioxidmolekylen (CO₂) innehåller två polära kovalenta bindningar mellan kol och syre. Trots detta är koldioxidmolekylen som helhet opolär. Vad beror detta på? Ringa in ett alternativ (1p).
- Molekylen är linjär och symmetrisk, vilket gör att dipolmomenten tar ut varandra.
- Kolatomen har fyra valenselektroner medan syre har sex, vilket skapar en perfekt elektronbalans.
- Syreatomerna är mer elektronegativa än kolatomen, vilket gör hela molekylen negativt laddad.
- De polära bindningarna är mycket svaga och påverkar inte molekylens totala polaritet.
- Svaveldioxid (SO2) bildas vid förbränning av fossila bränslen och bidrar till försurning. Vilken form har SO₂-molekylen? Ringa in ett alternativ (1p).
- Tetraedrisk
- Trigonal plan
- Linjär
- Vinklad
- Glycerol är en trögflytande vätska som används i bland annat hudkräm. Du kan se strukturformeln för glycerol i bilden till höger. Glycerol har en mycket hög kokpunkt (290 °C) för att vara en så pass liten molekyl. Vilken typ av bindningar är främst ansvariga för att hålla ihop glycerolmolekylerna i vätskefas? Ringa in ett alternativ (1p).
- Jonbindningar
- Jon–dipol-bindningar
- Vätebindningar
- van der Waals-bindningar
- Syrgas är en opolär molekyl, medan vatten är ett starkt polärt lösningsmedel. Ändå kan fiskar andas tack vare den lilla mängd syre som löser sig. Vilken typ av intermolekylär bindning uppstår mellan vattenmolekylerna och syrgasmolekylerna när syret löser sig? Ringa in ett alternativ (1p).
- Det uppstår en form av van der Waals-bindningar mellan syrgas- och vattenmolekylerna.
- Det uppstår jon–dipol-bindningar eftersom syrgasen joniseras när den kommer i kontakt med vatten.
- Det bildas starka vätebindningar mellan syrgasens atomer och vattnets väteatomer.
- Det bildas kovalenta bindningar mellan syrgasen och vattnet, vilket skapar den tillfälliga molekylen H2O3.
- Använd nedanstående elektronegativitetsvärden för att avgöra vilken av följande molekyler som innehåller den mest polära kovalenta bindningen.
Elektronegativitetsvärden:- H = 2,1
- C = 2,5
- N = 3,0
- O = 3,4
- F = 4,0
Ringa in ett alternativ. (1p)
- Vätefluorid (HF)
- Metan (CH4)
- Vatten (H2O)
- Ammoniak (NH3)
Del III. Frågor som kräver ett utredande svar
- PFAS-ämnen är en grupp av ämnen som är mycket vitt spridda i vår miljö, och används i allt från teflonpannor och vattenavstötande textilier till brandsläckningsmedel. De är dock också miljögifter och misstänks till exempel kunna ge hormonrubbningar och öka risken för cancer.
För att rena vatten från PFAS-ämnen används ofta filtrering genom aktivt kol. Aktivt kol liknar grafit till uppbyggnaden (se bild nedan till höger), men har behandlats så att lagren av kol inte ligger parallellt med varandra, utan så att säga har knycklats samman. Det gör att det aktiva kolet får porer med en mycket större inre yta.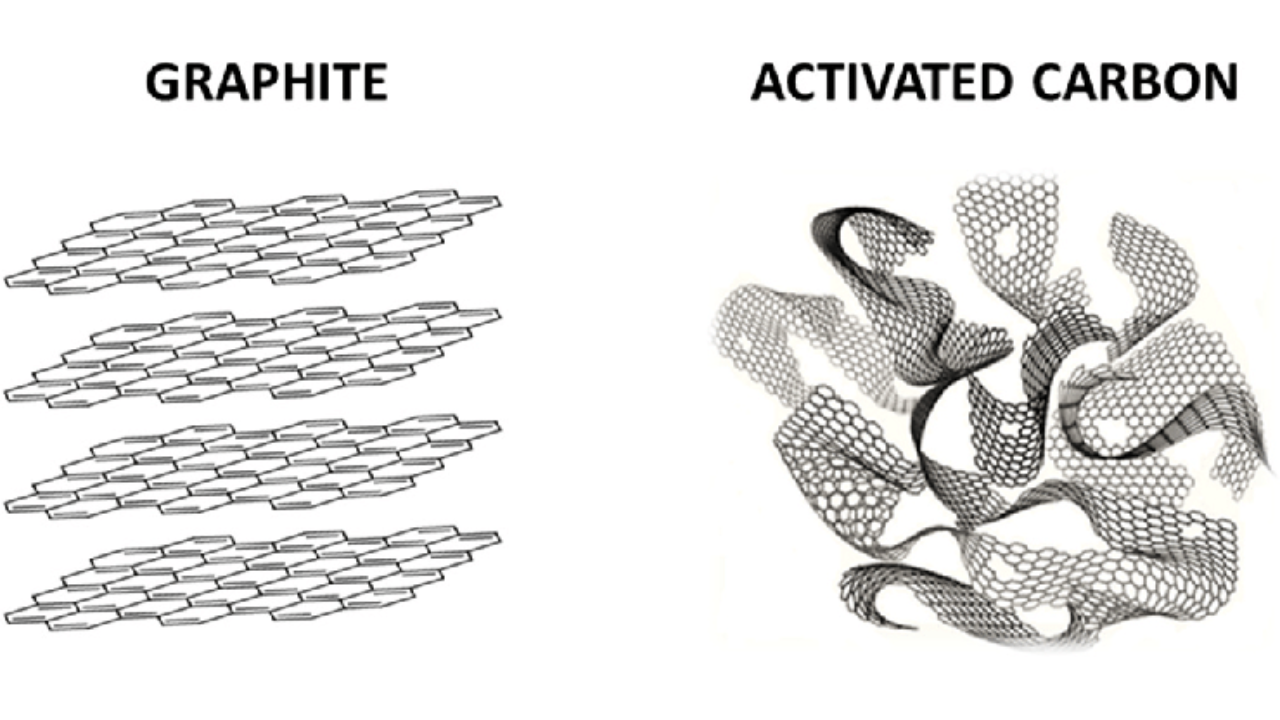
I bilden nedan visas strukturformeln för perfluorooktansyra (PFOA) och trifluorättiksyra (TFA), två vanligt förekommande PFAS-ämnen.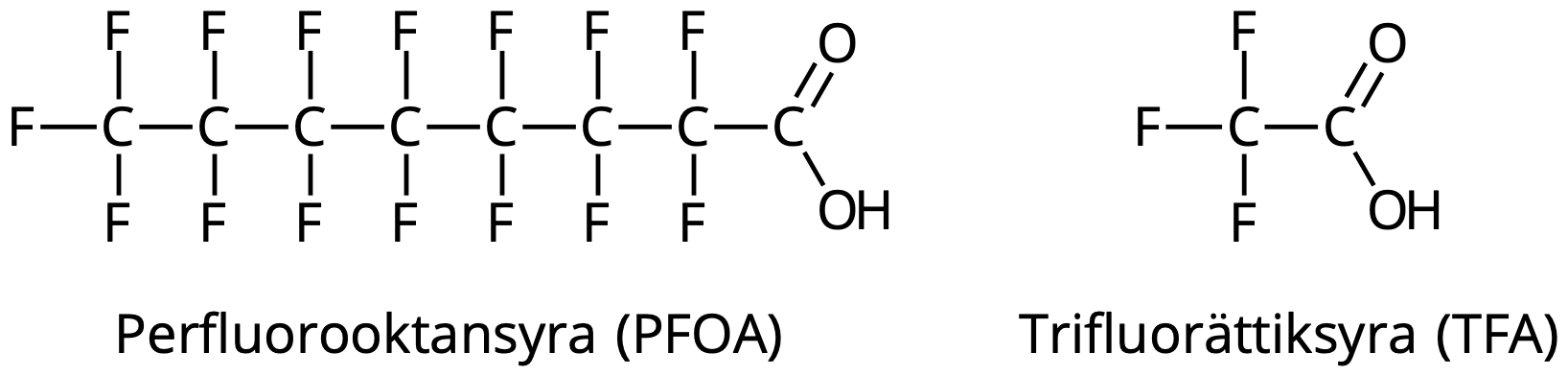
- Förklara vad som händer med PFOA när vatten som förorenats av PFOA får passera genom ett filter av aktivt kol, och hur vattnet renas. (4p)
Svara med utgångspunkt i- kemisk bindning och
- informationen som ges i frågan.
- Det är mycket svårare att rena vatten från TFA än från PFOA. Förklara varför det är så. Svara även här med utgångspunkt i kemisk bindning och informationen som ges i frågan. (3p)
- Förklara vad som händer med PFOA när vatten som förorenats av PFOA får passera genom ett filter av aktivt kol, och hur vattnet renas. (4p)
- I ett försök skulle man bestämma kristallvattenhalten i hafniumtetrafluorid, HfF4 · xH2O. Man hettade upp 1,02g av saltet och vägde hur mycket hafniumtetrafluorid som fanns kvar när allt vatten avdunstat. Den vattenfria hafniumtetrafluoriden vägde 0,841g. Vilken var den kristalliserade hafniumtetrafluoridens formel? (3p + 2p Språk och kommunikation)
Facit
Betygsgränser
Max: 27
Medel: 20,8 (B)
E: 11,0
D: 15,0
C: 18,0
B: 20,0
A: 23,0
Del I. Frågor som bara kräver ett kort svar (ett ord eller 1–2 meningar)
- 152,14u
Lösning: \(m_\mathrm{C_8H_8O_3} = (12,01 \cdot 8 + 1,008 \cdot 8 + 16,00 \cdot 3)\mathrm{g/mol} = 152,144\mathrm{u} ≈ 152,14\mathrm{u}\)
Kommentar: Svar utan enhet/fel enhet ger noll poäng. - 0,0112mol
Lösning: \(n_\mathrm{VBr_3} = \frac {m_\mathrm{VBr_3}}{M_\mathrm{VBr_3}} = \frac {3,25\mathrm{g}}{(50,94 + 79,90 \cdot 3)\mathrm{g/mol}} = 0,01118222\mathrm{mol} ≈ 0,0112\mathrm{mol}\)
Kommentar: Svar utan enhet/fel enhet ger noll poäng. - C3H8 + 5O2 → 3CO2 + 4H2O
- 17,1mol
Lösning\[\begin{aligned} n_\mathrm{NO_2}:n_\mathrm{O_2} &= 4:7 \\ n_\mathrm{O_2} &= \frac {7}{4} \cdot n_\mathrm{NO_2} = \frac {7}{4} \cdot 9,78\mathrm{mol} = 17,115\mathrm{mol} ≈ 17,1\mathrm{mol}\end{aligned}\]Kommentar: Även svar med fler eller färre gällande siffror godtas.
Del II. Flervalsfrågor
- d
- b
Förklaring: Kvarts är en nätverksmolekyl. För att smälta ämnet måste de starka kovalenta bindningarna mellan kisel- och syreatomerna i hela strukturen brytas, vilket förklarar den extremt höga smältpunkten.
van der Waals-bindningar och dipol–dipol-bindningar är orimliga eftersom de är jämförelsevis svaga bindningar, och inte skulle kunna ge upphov till en smältpunkt på 1 700 °C. Metallbindningar utesluts eftersom varken kisel eller syre är någon metall. - d
- d
- d
- b
Förklaring: Starka jonbindningar utesluts, då det krävs så mycket energi att bryta dem, och det skulle frigöras lika mycket energi när de bildas. Vätebindningar är typiskt ”klibbiga”, vilket anges i informationen i frågan att det inte är. Kovalenta bindningar är också orimligt, eftersom det skulle krävas så mycket energi att bryta dem, och det skulle frigöras lika mycket när de bildas. - a
- d
Förklaring: För att alla atomer i svaveldioxid ska uppnå ädelgasstruktur måste svaveldioxiden ha följande strukturformel: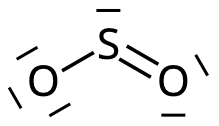
Eftersom det är tre elektrontäta områden kring svavelatomen blir molekylen vinklad. - c
- a
- a
Del III. Utredande frågor
- PFOA är en till största delen en opolär molekyl. Lagren av kol i det aktiva kolet är också opolära. Därför kan PFOA binda till kollagren med van der Waals-bindningar. Därmed avlägsnas PFOA från vattnet.
Bedömning
+1p – Eleven konstaterar att PFOA till största delen är opolär.
+1p – Eleven konstaterar att det aktiva kolet är opolärt.
+1p – Eleven anger att det uppstår bindningar mellan PFOA och aktivt kol.
+1p – Eleven nyanserar sitt svar med att det uppstår van der Waals-bindningar mellan PFOA och aktivt kol. - På grund av den korta kolkedjan är TFA en mycket mer polär molekyl än PFOA. Därför binder TFA-molekylen gärna till vattenmolekyler med dipol–dipol-bindningar och vätebindningar. Dessa bindningar är starkare än van der Waals-bindningar. (Detta gör att TFA är mer likt vatten.) Därför löser sig TFA hellre i vatten än i det aktiva kolet. Det medför att det är svårare att rena TFA från vatten än PFOA.
Bedömning
+0,5p – Eleven konstaterar att TFA är en mycket mer polär molekyl än PFOA.
+0,5p – Eleven nyanserar sitt svar genom att förklara varför TFA är mer polärt än PFOA.
+0,5p – Eleven konstaterar att det uppstår bindningar mellan TFA och vattenmolekyler.
+0,5p – Eleven nyanserar sitt svar genom att ange att det uppstår dipol–dipol-bindningar och/eller vätebindningar mellan TFA och vattenmolekyler.
+1p – Eleven konstaterar
* att dipol–dipol-bindningar (eller vätebindningar är starkare än van der Waals-bindningar
eller
* att TFA-molekyler är mer lika vattenmolekyler än aktivt kol,
och därför hellre löser sig i vattnet än i det aktiva kolet.
Kommentar: Om man även gått igenom syra-basreaktioner med sina elever kan svaret nyanseras ytterligare med att TFA-molekylen protolyseras, vilket ytterligare ökar lösligheten i vatten.
- PFOA är en till största delen en opolär molekyl. Lagren av kol i det aktiva kolet är också opolära. Därför kan PFOA binda till kollagren med van der Waals-bindningar. Därmed avlägsnas PFOA från vattnet.
- Lösning
\[\begin{aligned}n_\mathrm{HfF_4} &= \frac {m_\mathrm{HfF_4}}{M_\mathrm{HfF_4}} = \frac {0,841\mathrm{g}}{(178,5 + 19,00 \cdot 4)\mathrm{g/mol}} = 0,00330452\mathrm{mol} \\ n_\mathrm{H_2O} &= \frac {m_\mathrm{H_2O}}{M_\mathrm{H_2O}} = \frac {(1,02 - 0,841)\mathrm{g}}{(1,008 \cdot 2 + 16,00)\mathrm{g/mol}} = 0,00993561\mathrm{mol} \\ \frac {n_\mathrm{H_2O}}{n_\mathrm{HfF_4}} &= \frac {0,00993561\mathrm{mol}}{0,00330452\mathrm{mol}} = 3,00667474 ≈ 3\end{aligned}\]Alltså måste den rätta formeln vara HfF4 · 3H2O.Bedömning
+1p – Korrekt beräkning av \(n_\mathrm{HfF_4}\).
+1p – Korrekt beräkning av \(n_\mathrm{H_2O}\).
+1p – Korrekt beräkning av formeln HfF4 · 3H2OBedömning, språk och kommunikation
+1p – Eleven redovisar korrekt någon enhet som inte anges i uppgiften.
+1p – Eleven redovisar en tydlig beräkning med storhet, mätetal och enhet redovisas i väsentliga delar av uppgiften.