Tid: 90 minuter
Tillåtna hjälpmedel: Miniräknare, medföljande periodiskt system.
Hoppa direkt till …
Del I. Frågor som bara kräver ett kort svar (ett ord eller 1–2 meningar)
Längre svar ger risk för avdrag.
- Vad kan du om ämnena i det periodiska systemet: Vilka av grundämnena Al, Ar, Cl, Cu, Mg, Ne, P, Pb, S, Si är det som beskrivs nedan? Skriv rätt grundämne vid respektive beskrivning. Några av grundämnena blir över, något kanske beskrivs flera gånger. Skriv bara ett grundämne per rad.
- Detta grundämne är en alkalisk jordartsmetall. (1p)
- Detta grundämne används bland annat för att lysa upp reklamskyltar. (1p)
- Detta grundämne bildar en extremt hård oxid. (1p)
- Detta grundämne är i sin rena form en mycket giftig gas. (1p)
- Hur många elektroner i p-orbitaler har en fosforatom (räkna med alla p-orbitaler i alla skal)? (1p)
- Många metaller kan reagera med vatten.
- Vilken av följande metaller reagerar minst kraftigt med vatten? Ringa in ett alternativ. (1p)
- Na
- Mg
- K
- Skriv en reaktionsformel för när den valda metallen reagerar med vatten. Reaktionsformeln ska vara balanserad med minsta möjliga heltalskoefficienter. (2p)
- Vilken av följande metaller reagerar minst kraftigt med vatten? Ringa in ett alternativ. (1p)
- Vad heter föreningen K2CO3? (1p)
- Skriv formeln för strontiumnitrat. (1p)
- Skriv elektronformeln för cyanidjonen, CN–, och visa varför den är envärt negativ. (2p)
Del II. Ringa in de rätta svaren
Tips 1: Läs igenom alla svarsalternativen innan du bestämmer dig för vilket alternativ som är korrekt.
Tips 2: Om det är någon eller några frågor som du inte kan lösa direkt eller nästan direkt, så hoppa över dem så länge. Återkom till de frågorna senare, så vet du hur mycket tid du kan disponera på dem.
- Vilken av följande partiklar har elektronkonfigurationen 1s2 2s2 2p6 3s2 3p6? Ringa in ett alternativ. (1p)
- K+
- F–
- Cl
- Na+
- Vilken av följande ädelgaser är tyngst (har högst atommassa), och har därför undersökts för specialtillämpningar som fönsterisolering? Ringa in ett alternativ. (1p)
- Neon (Ne)
- Xenon (Xe)
- Argon (Ar)
- Helium (He)
- Klor har elektronkonfigurationen [Ne] 3s² 3p5. Vad händer vid reduktion av klor? Ringa in ett alternativ. (1p)
- En elektron överförs till 4p-orbitalen eftersom 3p är full.
- En proton läggs till i kärnan för att balansera laddningen.
- En elektron läggs till i 3p-orbitalen, vilket ger en stabil ädelgasstruktur.
- En elektron läggs till i 3s-orbitalen så att det bildas en envärt negativ jon.
- Vad är sant om grundämnet fosfor? Ringa in ett alternativ. (1p)
- Fosfor är en silverglänsande metall som används i rostfritt stål.
- Det finns en röd form av fosfor, som används i tändsticksplån.
- Fosfor är en gas som används i lysrör för att ge ett starkt sken.
- Fosfor har sju valenselektroner.
- Vilket av följande ämnen är ett exempel på en jonförening? Ringa in ett alternativ. (1p)
- Väteklorid
- Natriumdivätefosfat
- Kvävemonoxid
- Koldioxid
- Magnesium reagerar med syre och bildar magnesiumoxid. Hur många elektroner avger respektive tar varje atom upp i reaktionen? Ringa in ett alternativ. (1p)
- Mg avger alla sina elektroner och blir en kärna; O tar upp dem och bildar en mycket stor anjon.
- Mg tar upp 6 elektroner för att fylla sitt M-skal; O avger sina 2 yttersta elektroner.
- Mg avger 1 elektron; O tar upp 1 elektron, vilket resulterar i Mg⁺ och O⁻.
- Mg avger 2 elektroner; O tar upp 2 elektroner.
- I vilken av nedanstående blandningar uppstår det en fällning? Ringa in ett alternativ. (1p)
- Mg(NO3)2(aq) + 2NaOH(aq) →
- CaI2(aq) + Mg(NO3)2(aq) →
- Ba(ClO3)2(aq) + 2NH4Cl(aq) →
- Na2SO4(aq) + 2NH4NO3(aq) →
- Du tillsätter en bariumjonlösning till en lösning med okänt innehåll, och ser att det genast bildas en vit fällning. Vad innebär det? Ringa in ett alternativ. (1p)
- Att den andra lösningen innehöll sulfatjoner.
- Att det är lämpligt att göra ett knallgastest på den andra lösningen.
- Att den andra lösningen innehöll kloridjoner.
- Att bariumjonerna har reducerats till bariummetall.
- Jonföreningar är ofta spröda och splittras lätt om man slår på dem. Vad är den huvudsakliga orsaken till denna sprödhet? Ringa in ett alternativ. (1p)
- Om jonlagren förskjuts så att lika laddningar hamnar bredvid varandra uppstår repulsion.
- Jonbindningarna är i själva verket mycket svaga och instabila vid mekanisk påverkan.
- De absorberar lätt fukt från luften, vilket gör kristallstrukturen skör och porös.
- De innehåller ofta mikroskopiska sprickor och defekter redan från början.
- Ju större en metallatom är, desto större yta är metallbindningen utspridd över, och desto svagare blir bindningen. Vad betyder detta för kokpunkterna på alkalimetallerna om vi rör oss neråt i alkalimetallgruppen? Ringa in ett alternativ. (1p)
- Kokpunkten ökar när vi rör oss neråt i alkalimetallgruppen.
- Kokpunkten minskar när vi rör oss neråt i alkalimetallgruppen.
- Kokpunkten är ungefär densamma för alla alkalimetallerna.
- Kokpunkten påverkas inte av styrkan i metallbindningen, utan av andra faktorer.
- Vilken typ av bindning finns mellan syreatomerna i en syremolekyl (O2)? Ringa in ett alternativ. (1p)
- En trippelbindning
- En jonbindning
- En dubbelbindning
- En enkelbindning
Del III. Frågor som kräver ett utredande svar
- Man kan ta reda på om ett ämne är en molekylförening eller en jonförening genom att testa om en vattenlösning av ämnet leder ström eller inte. I ett experiment prövar du att lösa 0,10 g fast silverklorid i 0,250 dm3 avjonat vatten och stoppar ner en ledningsprovare (doppelektrod med batteri och lampa). Den ger inget utslag. Det är dock inget fel på ledningsprovaren.
- Förklara vad det är som gör att man kan identifiera jon- och molekylföreningar med hjälp av en ledningsprovare. (3p)
- Förklara varför det inte blir något utslag i försöket med silverklorid. (1p)
- Förklara så utförligt och nyanserat som möjligt hur det kommer sig att metaller kan leda ström. Stötta din förklaring med en eller flera bilder. (4p)
Facit
Betygsgränser
Max: 31
Medel: 25,9 (B)
E: 14,0
D: 18,0
C: 23,0
B: 25,0
A: 28,0
Del I. Frågor som bara kräver ett kort svar (ett ord eller 1–2 meningar)
- Mg
- Ne
- Al
- Cl
- 9 st.
Lösning: Elektronkonfigurationen för fosfor är 1s2 2s2 2p6 3s2 3p3. Totalt kommer fosforatomen att ha 6 + 3 = 9 elektroner i p-orbitaler. -
- ii.
- Mg(s) + 2H2O → Mg(OH)2(aq) + H2(g)
Bedömning
+1p – Eleven identifierar att det bildas hydroxidjoner och vätgas.
+1p – Eleven skriver en helt korrekt balanserad reaktionsformel.
Kommentar: Aggregationstillstånden behöver inte sättas ut för poäng.
- Kaliumkarbonat
Kommentar: Även dikaliumkarbonat godtas. - Sr(NO3)2
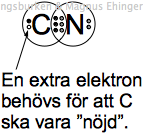
+1p – Bra bild, med tydlig trippelbindning.
+1p – Tydligt utpekande av/förklaring till ”extra” elektron (totalt tio elektroner visas).
Del II. Flervalsfrågor
- a
- b
- c
- b
- b
- d
- a
- a
- a
- b
- c
Del III. Utredande frågor
- För att föra vidare en elektrisk ström krävs det fria laddade partiklar. En jonförening i löst form bildar fria positiva och negativa joner. Det gör det inte en molekylförening. Därför kan den lösta jonföreningen leda ström, men inte molekylföreningen.
Bedömning
+1p – Eleven konstaterar att jonföreningar i vattenlösning kan leda ström, vilket inte molekylföreningar kan.
+1p – Eleven uppfyller kravet för 1p ovan, förklarar att det krävs fria laddade partiklar för att ström ska kunna ledas, och utvecklar förklaringen utifrån en av punkterna nedan.- Lösta jonföreningar bildar fria joner (laddade partiklar).
- Lösta molekylföreningar bildar inga fria laddade partiklar.
- Silverklorid är ett mycket svårlösligt salt. Därför bildas det i princip inga fria silver- och kloridjoner när den fasta föreningen blandas med vatten, och därför leder den inte någon ström.
Bedömning
+1p – Eleven förklarar utifrån att silverklorid är ett svårlösligt salt, och att det därför i princip ändå inte finns några joner som kan leda strömmen i lösningen.
- För att föra vidare en elektrisk ström krävs det fria laddade partiklar. En jonförening i löst form bildar fria positiva och negativa joner. Det gör det inte en molekylförening. Därför kan den lösta jonföreningen leda ström, men inte molekylföreningen.
- Bedömning
+1p – Elektronerna i en bit metall är delokaliserade.
+1p – I en bit metall sitter atomerna som positiva joner i ett enda stort elektronmoln.
+1p – Tack vare de delokaliserade elektronerna (elektronmolnet) kan metallen ta upp en elektron.
+1p – Överskottet på elektroner gör att en annan elektron åker ut i andra änden av metallen, och därigenom skapas en elektrisk ström.