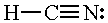 Enkel-, dubbel- och trippelbindningar
Enkel-, dubbel- och trippelbindningar
Vätgas
 Väteatomerna delar på ett enda elektronpar: H–H
Väteatomerna delar på ett enda elektronpar: H–H
- Enkelbindning
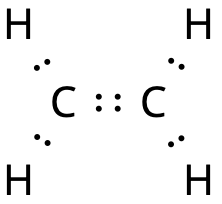
Eten
Kolatomerna delar på två elektronpar: H2C=CH2
- Dubbelbindning
Kvävgas
Rita upp elektronformeln för N2
Kväveatomern delar på tre elektronpar: N≡N
- Trippelbindning
Atomjoner och sammansatta joner
Salter av atomjoner
Jonerna består endast av ett atmoslag
- Exempel: Na+Cl–
Sammansatta joner
Jonerna består av flera atomslag
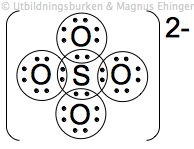
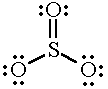
Exempel: Sulfatjonen, SO\(_4^{2-}\)
Fyra syreatomer binder till en svavelatom
Hela strukturen är tvåvärt negativ
Kopparsulfat: CuSO4 innehåller en atomjon (Cu2+) och en sammansatt jon (SO\(_4^{2-}\)).
Exempel: Kalciumkarbonat, CaCO3
Karbonatjonen är tvåvärt negativ
Visa hur karbonatjonerna, \({\sf \text{CO}_3^{2-}}\) sitter i förhållande till calciumjonerna, Ca2+ i modellen.
Hur kan man räkna ut strukturen på en molekyl?
Rita elektronformeln för molekylen
Sätt ut en central atom, och rita upp atomer runt denna
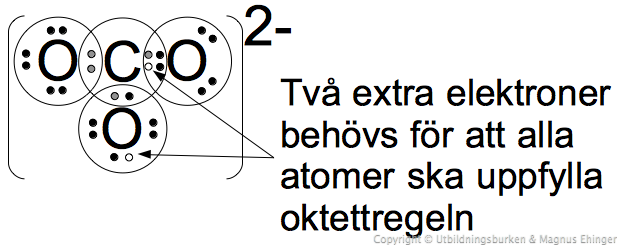
- Exempel: CO2
- Sätt kolet i mitten, syreatomerna vid sidan av: O C O
Flytta in elektroner mellan atomerna, så att alla atomer uppnår ädelgasstruktur
- Exempel:

- Eftersom kol har 4 valenselektroner, har två elektroner från vardera syret flyttats in för att ge kolet ädelgasstruktur. Samtidigt lånar kolet ut två av sina elektroner till vardera syreatomen så att dessa också får ädelgasstruktur.
Räkna antalet områden med hög elektrontäthet runt centralatomen
- Enkelbindningar, dubbelbindningar och trippelbindningar räknas som ett område med hög täthet.
- Ett fritt elektronpar räknas som ett område med hög täthet
I exemplet med koldioxid
- Vi har två områden med hög elektrontäthet runt centralatomen
- Eftersom elektronparen ogillar varandra, vill de vara så långt ifrån varandra som möjligt
- Därför blir strukturen linjär
Exempel: vätecyanid, HCN
- Rita elektronformeln
- Räkna områdena med hög elektrontäthet runt centralatomen
- De är två stycken
- Alltså är molekylen linjär